Imaginează-ți că ai o telecomandă ce poate controla creierul pornind și oprind celulele nervoase doar cu ajutorul luminii. Aceasta este optogenetica, o tehnologie inovatoare care combină genetica și lumina pentru a controla activitatea neuronală. Proteine fotosensibile sunt introduse în celulele nervoase și ele permit cercetătorilor să activeze sau să inhibe neuronii specifici prin expunerea la lumina de anumite lungimi de undă.
În anii 1990 laureatul Nobel Francis Crick, cunoscut pentru descoperirea structurii ADN-ului a sugerat că pentru a descifra misterele creierului uman ar trebui să dezvoltăm metode precise pentru a controla celulele cerebrale. Această viziune futuristă a început să prindă contur la începutul anilor 2000 când cercetătorii au descoperit primele proteine fotosensibile capabile să răspundă la lumină.
Canalrhodopsina-2 (ChR2), o proteină derivată din alge unicelulare a fost descoperită și utilizată de Peter Hegemann și Georg Nagel. Dar adevărata revoluție a început atunci când Gero Miesenböck a demonstrat în 2002 că aceste proteine pot fi folosite pentru a controla activitatea neuronală în organisme vii.
„Imaginați-vă cum ar fi să putem porni și opri, din exterior, neuronii din creierul unui animal. Sună ca și cum ați transforma creatura într-un fel de robot, ca într-o povestire science-fiction, nu?”

Gero Miesenböck
Director Centru pentru Circuite Neuronale și Comportamentale, Universitatea din Oxford
Această idee, deși la vremea respectivă părea desprinsă dintr-un scenariu SF a început să prindă contur în cercetarea neuroștiințifică. Miesenböck nu a fost singur în această aventură, în paralel la Stanford, Karl Deisseroth și Ed Boyden au rafinat tehnica arătând că ChR2 poate fi utilizată pentru a activa neuronii în țesutul mamiferelor. În 2005 echipa lor a publicat o serie de lucrări care au stabilit optogenetica ca pe un instrument esențial în arsenalul neuroștiințific.
Cum funcționează
Cercetătorii introduc proteine sensibile la lumină cum ar fi canalrhodopsina-2 (ChR2) în celulele nervoase. Aceste proteine derivate din alge reacționează la lumina albastră. Când neuronii sunt expuși la o anumită lumină, proteinele se deschid și permit ionilor să intre sau să iasă din celulă. Fibrele optice implantate lângă neuronii țintă transmit lumina care activează sau oprește neuronii, modulând semnalele de durere. Ajustarea intensității, frecvenței și duratei luminii permite personalizarea tratamentului.
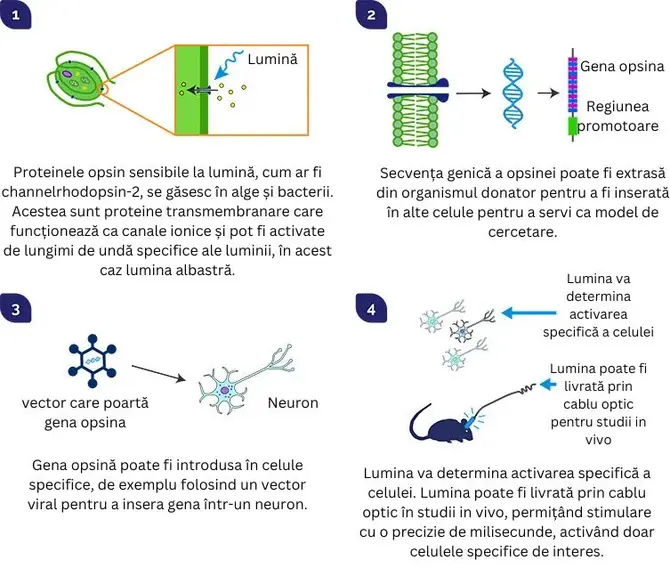
Aplicații ale optogenetice
Studiul circuitelor neuronale
Optogenetica oferă un instrument puternic pentru înțelegerea circuitelor neuronale complexe. Utilizând proteine fotosensibile pentru a regla activitatea specifică a neuronilor, cercetătorii sunt capabili să cartografieze conexiunile neuronale și să analizeze modul în care acestea afectează comportamentul și funcționarea globală a creierului. Acest nivel de precizie permite studierea modului în care diferite regiuni ale creierului interacționează și contribuie la procesele cognitive și motorii.
Controlul comportamentului la animale
Prin activarea sau inhibarea specifică a neuronilor responsabili de anumite comportamente, optogenetica a revoluționat studiul comportamentului animalelor. De exemplu, cercetătorii pot induce sau suprima comportamente precum anxietatea, foamea sau reacțiile la frică prin expunerea la lumină a anumitor regiuni cerebrale. Aceste experimente ajută la înțelegerea bazelor neurologice ale comportamentelor complexe și pot contribui la dezvoltarea de noi terapii pentru tulburările comportamentale.
Tratarea tulburărilor neurologice
Tehnologia are un potențial semnificativ în cercetarea și tratamentul bolii Parkinson. Prin stimularea sau inhibarea precisă a neuronilor dopaminergici afectați, cercetătorii pot ameliora simptomele motorii caracteristice acestei boli. Aceste intervenții pot duce la dezvoltarea unor terapii mai eficiente și mai puțin invazive decât stimularea cerebrală profundă, oferind pacienților o calitate a vieții îmbunătățită.
În cazul bolii Alzheimer, optogenetica permite cercetătorilor să exploreze modul în care depunerile de amiloid și tau afectează funcționarea neuronală și să testeze noi abordări terapeutice. Prin manipularea activității neuronale în modelele animale se pot identifica mecanismele de bază ale declinului cognitiv și se pot dezvolta strategii pentru încetinirea sau inversarea progresiei bolii.
Reglarea ritmului circadian
Oferă o metodă precisă pentru studierea și reglarea ritmurilor circadiene. Prin controlul activității neuronale în nucleul suprachiasmatic, regiunea creierului responsabilă de ritmurile circadiene cercetătorii pot influența ciclurile de somn-veghe. Aceasta deschide calea pentru noi tratamente pentru tulburările de somn, cum ar fi insomnia și sindromul de fază întârziată a somnului.
Cardiologie și endocrinologie
În cardiologie poate fi utilizată pentru a controla ritmul cardiac prin stimularea specifică a celulelor cardiace. Aceasta poate ajuta la tratarea aritmiilor și altor tulburări de ritm cardiac fără a necesita implanturi electrice invazive.
Optogenetica permite controlul precis al secreției hormonale prin manipularea activității glandelor endocrine. Aceasta poate fi utilizată pentru studierea și tratarea tulburărilor hormonale, oferind o alternativă la terapiile hormonale tradiționale.
Ingineria țesuturilor și regenerarea organelor
Aceasta joacă un rol important în regenerarea și reabilitarea țesuturilor musculare și nervoase. Prin stimularea specifică a celulelor stem și a altor tipuri de celule, cercetătorii pot promova creșterea și dezvoltarea țesuturilor necesare pentru repararea leziunilor sau pentru tratarea bolilor degenerative. Astfel se deschid noi perspective pentru tratamentele personalizate și pentru recuperarea funcțiilor pierdute. Cum anume funcționează:
- Cu ajutorul luminii, cercetătorii pot activa celule specifice pentru a le face să crească și să se dezvolte în tipuri de țesuturi necesare. De exemplu, pot stimula celulele stem să devină celule musculare sau neuronale.
- În timpul dezvoltării unui organism, celulele trebuie să se organizeze în moduri foarte precise. Optogenetica permite cercetătorilor să ghidze aceste celule, asigurându-se că se formează structuri corecte și funcționale.
- În cazul unor leziuni sau boli, optogenetica poate ajuta la regenerarea țesuturilor deteriorate. Cercetătorii pot folosi lumina pentru a stimula creșterea de noi celule în zona afectată, ajutând astfel la vindecare.
- Uneori, în timpul dezvoltării, pot apărea anomalii sau defecte. Această metodă permite cercetătorilor să corecteze aceste probleme prin ajustarea activității celulelor în timp real. De exemplu, pot folosi lumina pentru a întări sau relaxa anumite părți ale țesutului, prevenind astfel formarea incorectă.
Terapie pentru dureri și restaurarea funcțiilor senzoriale
Oferă un control precis asupra surselor de durere fără a afecta teoretic alte funcții ale corpului. Tehnologia permite activarea sau inhibarea neuronilor specifici ceea ce duce la ameliorarea durerii fără efectele secundare asociate cu analgezicele tradiționale precum somnolența, constipația și riscul de dependență. Spre deosebire de analgezicele clasice care afectează întregul sistem nervos central încearcă să țintească precis doar neuronii responsabili de durere minimizând astfel impactul asupra altor funcții corporale. Optogenetica a fost utilizată pentru a restabili vederea la pacienții cu retinită pigmentară, o boală degenerativă a retinei prin introducerea opsinelor în celulele retiniene.
Cercetarea funcțiilor cerebrale
Tehnologia permite cercetătorilor să manipuleze specific neuronii pentru a studia modul în care aceștia contribuie la funcțiile cognitive și comportamentale. Aceasta include studiul memoriei, emoțiilor și comportamentului.
Riscuri și complicații
Complicațiile pot include infecții, inflamații sau leziuni tisulare în jurul zonei de implantare. Implanturile optice necesare pentru terapia optogenetică pot cauza reacții adverse. De exemplu există riscul de reacții ale țesuturilor la materialele implantate precum și posibile complicații mecanice ale dispozitivului. În plus, pe termen lung, implanturile trebuie monitorizate și în unele cazuri pot necesita înlocuire sau ajustare.
Activarea sau inhibarea greșită a neuronilor poate duce la probleme neurologice grave afectând funcțiile motorii și cognitive. Proteinele fotosensibile și utilizarea constantă a luminii asupra neuronilor sunt încă noi pentru știință nu există suficiente studii pe termen lung pentru a înțelege pe deplin efectele și potențialele daune ale acestei tehnologii. Deși a avut rezultate promițătoare în studii preclinice și unele clinice, siguranța și eficacitatea pe termen lung sunt încă sub investigație. Utilizarea excesivă sau necorespunzătoare a luminii poate supra-stimula neuronii ducând la stres celular și posibile daune neuronale.
Studii și cercetări recente
Un studiu publicat în Journal of Neuroscience a explorat utilizarea optogeneticii pentru ameliorarea durerii neuropatice la modele animale. Cercetătorii au reușit să activeze specific neuronii inhibitori din măduva spinării folosind lumină, ceea ce a dus la o reducere semnificativă a percepției durerii . Această abordare nu doar că oferă un control precis asupra durerii, dar reduce și necesitatea medicamentelor tradiționale.
Un alt studiu realizat de echipa de la Massachusetts Institute of Technology (MIT) a demonstrat că optogenetica poate fi utilizată pentru a modula activitatea cerebrală în zonele asociate cu durerea cronică. Utilizând șoareci de laborator, cercetătorii au reușit să blocheze semnalele dureroase prin stimularea cu lumină a anumitor celule nervoase, ceea ce a dus la o ameliorare semnificativă a simptomelor dureroase. Aceste rezultate promit o abordare non-invazivă și eficientă pentru pacienții care suferă de durere cronică.
Un studiu recent realizat de cercetătorii de la Harvard Medical School a demonstrat utilizarea optogeneticii pentru a controla activitatea neuronală implicată în durerea cronică la modelele animale. Cercetătorii au utilizat opsine specifice, introduse genetic în neuroni pentru a activa sau inhiba acești neuroni cu ajutorul luminii. Acest studiu a arătat că activarea optogenetică a opsinelor “off” poate reduce sensibilitatea la durere și răspunsurile la stimuli dureroși la șoareci cu leziuni cronice .
Într-un alt exemplu, laboratorul lui Scott Delp de la Stanford University a reușit să implementeze optogenetica pentru a trata durerea cronică periferică la șoareci. Aceștia au utilizat viruși non-patogeni pentru a introduce opsine în nervul sciatic al șoarecilor, permițând activarea cu lumină pentru a reduce durerea. Această tehnică a demonstrat potențialul de a fi adaptată pentru utilizare umană, indicând o posibilitate promițătoare pentru viitoarele tratamente ale durerii la oameni .
De asemenea, o colaborare între laboratoarele lui Robert Gereau și John Rogers a dus la dezvoltarea unui sistem implantabil pentru livrarea wireless a luminii la măduva spinării și sistemul nervos periferic, facilitând terapia optogenetică. Acest sistem ușor și flexibil oferă o soluție practică pentru utilizarea continuă a optogeneticii la pacienții umani .
Optogenetica a fost testată și pe subiecți umani în câteva studii izolate
Restaurarea vederii:
- Un studiu publicat în 2021 a raportat succesul utilizării optogeneticii pentru a restabili parțial vederea la un pacient orb de 58 de ani. Acesta a implicat injectarea unei proteine sensibile la lumină în retina pacientului, care a permis pacientului să vadă imagini și obiecte în mișcare. Alte studii, precum cele derulate de Bionic Sight și GenSight, au arătat rezultate similare, unde pacienții cu retinită pigmentară au reușit să perceapă lumina și mișcarea.
Tulburările de mișcare:
- Deși majoritatea cercetărilor sunt încă în faza preclinică, există interese în utilizarea optogeneticii pentru a trata tulburările de mișcare, cum ar fi boala Parkinson. În aceste studii neuronii specifici din creier sunt modificați genetic pentru a răspunde la lumină, cu scopul de a restabili controlul motor.
Controlul durerii:
- Cercetările sunt în curs de desfășurare pentru a utiliza optogenetica în controlul durerii cronice. Aceasta implică modificarea neuronilor din măduva spinării sau alte regiuni ale sistemului nervos central pentru a reduce percepția durerii.
Epilepsie:
- Studiile inițiale au explorat utilizarea optogeneticii pentru a controla crizele epileptice. Ideea este de a implanta celule sensibile la lumină în regiuni ale creierului implicate în generarea crizelor pentru a le inhiba activitatea prin iluminare controlată.
Comentarii ale experților din domeniu
Dr. Karl Deisseroth, unul dintre pionierii optogeneticii subliniază importanța acestei tehnologii:
“Optogenetica oferă o metodă fără precedent de a controla precis activitatea neuronală, ceea ce deschide noi orizonturi în tratamentul durerii cronice. Capacitatea de a targeta specific neuronii implicați în durere promite să revoluționeze modul în care abordăm tratamentul acestei afecțiuni debilitante”

Dr. Karl Deisseroth
Profesor de bioinginerie, de psihiatrie și științe comportamentale, Universitatea Stanford
“Tehnologia optogenetică are potențialul de a schimba radical tratamentul durerii, oferind soluții personalizate și eficiente fără efectele secundare ale medicamentelor convenționale. Suntem pe cale să transformăm managementul durerii cronice prin această abordare inovatoare”

Dr. Scott Delp
Profesor, Stanford University
Deși are un potențial imens în cercetare și medicină există riscuri și preocupări asociate cu această tehnologie. În primul rând modificările genetice necesare pentru a introduce proteinele sensibile la lumină ar putea avea efecte neprevăzute, declanșând răspunsuri imune sau alte reacții adverse iar inserția genelor în genom ar putea afecta funcțiile normale ale celulelor sau ar putea activa oncogene, ceea ce ar conduce la dezvoltarea cancerului. În plus, expunerea prelungită la lumină intensă necesară pentru a activa proteinele ar putea deteriora țesuturile în special retina care ar putea fi afectată de lumina intensă. Controlul și precizia sunt esențiale deoarece activarea optogenetică trebuie să fie extrem de precisă pentru a evita stimularea nedorită a altor celule sau țesuturi care ar putea duce la efecte secundare severe. În ceea ce privește efectele psihologice și comportamentale, manipularea neuronilor poate avea consecințe necunoscute asupra comportamentului și funcțiilor cognitive existând riscul de a declanșa tulburări psihice sau de comportament.
Pe lângă riscurile menționate există și povești de groază potențiale asociate cu optogenetica. Unul dintre cele mai mari temeri este legat de controlul mintal și etică. Într-un scenariu distopic, optogenetica ar putea fi folosită pentru a controla comportamentul oamenilor fără consimțământul lor ceea ce ar ridica probleme serioase de etică și libertate personală. De asemenea există riscul ca în timpul cercetărilor să apară accidente în care subiecții, fie animale, fie oameni în studii clinice să fie afectați grav de activările optogenetice necontrolate. Un alt scenariu îngrijorător este aplicarea greșită în terapie. Dacă nu este aplicată corect, ar putea agrava starea pacienților în loc să o îmbunătățească. De exemplu activarea accidentală a unor circuite neuronale greșite ar putea induce convulsii sau alte probleme neurologice.
Trebuie să abordăm cu mare precauție această tehnologie dat fiindcă nu înțelegem pe deplin potențialele ei efecte pe termen lung. Problemele etice precum manipularea conștiinței și comportamentului uman sunt profunde și nu pot fi trecute cu vederea — ele ridică întrebări serioase despre consimțământ, identitate și libertate personală. Deși promite transformări radicale în tratamentul afecțiunilor neurologice și înțelegerea funcției cerebrale, trebuie să fim vigilenți în fața riscurilor și dilemelor pe care le generează.
Citește mai multe despre inovații în sănătate aici
Referințe
- Sung, YL., Wang, TW., Lin, TT. et al. Optogenetics in cardiology: methodology and future applications. Int J Arrhythm 23, 9 (2022). https://doi.org/10.1186/s42444-022-00060-4
- Deisseroth, K. et al. “Optogenetics: Controlling the Brain with Light.” Scientific American, 305(5), 2011, pp. 48-55.
- Yizhar, O. et al. “Optogenetics in neural systems.” Neuron, 71(1), 2011, pp. 9-34.
- Boyden, E. S. et al. “Millisecond-timescale, genetically targeted optical control of neural activity.” Nature Neuroscience, 8(9), 2005, pp. 1263-1268.
- Chen W, Li C, Liang W, Li Y, Zou Z, Xie Y, Liao Y, Yu L, Lin Q, Huang M, Li Z, Zhu X. The Roles of Optogenetics and Technology in Neurobiology: A Review. Front Aging Neurosci. 2022 Apr 19;14:867863. doi: 10.3389/fnagi.2022.867863. PMID: 35517048; PMCID: PMC9063564.
- Shirai F, Hayashi-Takagi A. Optogenetics: Applications in psychiatric research. Psychiatry Clin Neurosci. 2017 Jun;71(6):363-372. doi: 10.1111/pcn.12516. Epub 2017 Mar 30. PMID: 28233379.
- Stuber, G., Sparta, D., Stamatakis, A. et al. Excitatory transmission from the amygdala to nucleus accumbens facilitates reward seeking. Nature 475, 377–380 (2011). https://doi.org/10.1038/nature10194
- Zhang, F., Aravanis, A., Adamantidis, A. et al. Circuit-breakers: optical technologies for probing neural signals and systems. Nat Rev Neurosci 8, 577–581 (2007). https://doi.org/10.1038/nrn2192
- Deisseroth K, Etkin A, Malenka RC. Optogenetics and the circuit dynamics of psychiatric disease. JAMA. 2015 May 26;313(20):2019-20. doi: 10.1001/jama.2015.2544. PMID: 25974025; PMCID: PMC4775737.
- Dieter A, Keppeler D, Moser T. Towards the optical cochlear implant: optogenetic approaches for hearing restoration. EMBO Mol Med. 2020 Apr 7;12(4):e11618. doi: 10.15252/emmm.201911618. Epub 2020 Mar 30. PMID: 32227585; PMCID: PMC7136966.
- Faltus T, Freise J, Fluck C, Zillmann H. Ethics and regulation of neuronal optogenetics in the European Union. Pflugers Arch. 2023 Dec;475(12):1505-1517. doi: 10.1007/s00424-023-02888-8. Epub 2023 Nov 24. PMID: 37996706; PMCID: PMC10730653.




